Strukturní izomery jsou to, co
V tomto článku budeme hovořit o strukturních izomerech, charakteristikách jejich struktury a typech isomerismu. Podívejme se podrobně na samotný fenomén isomerismu a ukážeme také jejich využití v životě.
Fenomén isomerismu
Izomerismus je zvláštní fenomén, který předurčujeexistence chem. sloučeniny, stejné isomery, látky s identickými složeními atomů a molekulární hmotností, které se liší pouze atomovým uspořádáním v prostoru nebo struktuře, což vede ke změně a získávání různých nových vlastností. Strukturní izomery jsou látky vytvořené v důsledku takové změny polohy atomů v prostoru, které budou podrobněji popsány níže.
Pokud jde o isomerismus, stojí za to pamatovat existenci takového procesu, jakým je izomerizace, což je proces přechodu jednoho izoméru na druhý v důsledku chem. transformací.
Druhy isomerismu
Isomerism valence je druh izomerní struktury, ve kterém je přenos izomerů sami (jeden do druhého) možný jako výsledek přerozdělení valenčních vazeb.
Izomerie je situace u stejného typu látky uhlíkového skeletu, ale různými funkcemi polohy. Pozoruhodným příkladem je kyselina 2- a 4-chlorbutan.
Interklasová izomerie zakrývá rozdíl mezi izomery v povaze funkčních skupin.
Metamerismus je rozložení polohy atomůuhlík mezi určitým počtem uhlíkových radikálů, heteroatom molekuly slouží jako oddělovač. Tento druh isomerismu je charakteristický pro aminy, thiosféry, étery, a to jak jednoduché, tak složité.
Isomerismus uhlíkového skeletu je rozdílpolohy atomů uhlíku, nebo spíše jejich pořadí. Například: fenantren a antracen mají obecný vzorec C14H10, ale různé typy redistribuce valenčních vazeb.
Strukturní izomery
Strukturní izomery jsou látky, které majípodobný vzorec pro strukturu hmoty, ale liší se podle vzorce molekuly. Strukturní izomery - typ látek, které jsou z hlediska kvantitativního a kvalitativního složení navzájem identické, avšak pořadí atomové vazby (chemická struktura) je odlišné.
Strukturní izomery jsou klasifikovány podle typu izometrické struktury, jejichž typy jsou uvedeny výše, v položce o typech isomerismu.
Strukturní vzorec látky izomer máširoká škála modifikací. Některé příklady isomerie mohou být látky, jako je například kyselina butanová, kyselina 2-methylpropanové, methylpropionát, dioxanu, ethyl-acetát, isopropyl-formiát mají stejné složení všech tří typů atomů složené z látek, ale liší se v poloze atomů ve sloučenině.

Dalším jasným příkladem isomerismu je existence pentanu, neopentanu a isopentanu.
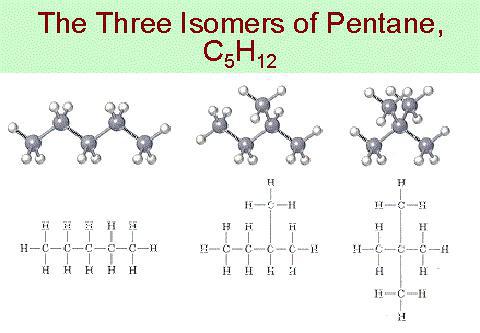
Názvy izomerů
Jak již bylo zmíněno dříve, strukturní izomery jsoulátky, které mají podobný vzorec pro strukturu látky, ale liší se ve vzorci molekuly. Takové sloučeniny mají klasifikaci, která odpovídá vlastnostem jejich vlastností, struktuře a poloze atomů v molekule izomeru, rozdílům v počtu funkčních skupin, valenčním vazbám, přítomnosti atomů určitého prvku v látce atd. Názvy strukturních izomerů se získávají různými způsoby. Zvažte to pro příklad 3-methylbutanolu 1, jako zástupce alkoholů.
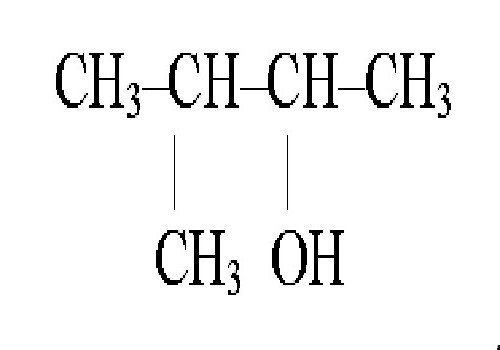
V případě alkoholů, když se získá názevalkoholy začínají volbou řetězce uhlíku, který je dominantní, číslování, jehož účelem je přiřadit nejmenší možné číslo skupině OH, přičemž se přihlédne k pořadí. Samotné jméno začíná být složeno ze substituentu v uhlíkovém řetězci, za ním následuje jméno hlavního řetězce, za ním následuje přípona -ol a obrázek označuje atom uhlíku spojený s OH skupinou.
</ p>

