Chemická vazba a princip její tvorby
Chemická vazba je poměrně složitá koncepce,který byl založen na dlouhou dobu na základě učení a představ o struktuře atomu. Takže v XVI-XVII století. byly první pokusy vysvětlit chemickou podobnost na základě korpuskulární teorie. R. Boyle si myslel, že hnací silou chemických reakcí je shoda náhodných částic, jako je zámek klíčů, tj. Atomy "shromážděné" a "rozložené", které tvoří nové látky. Později ve století XVIII. na nahrazení mechanické teorie přijde dynamika, příznivcem kterého byl I. Newton. Věřil, že příčinou chemické podobnosti jsou síly přitažlivosti s různou intenzitou.
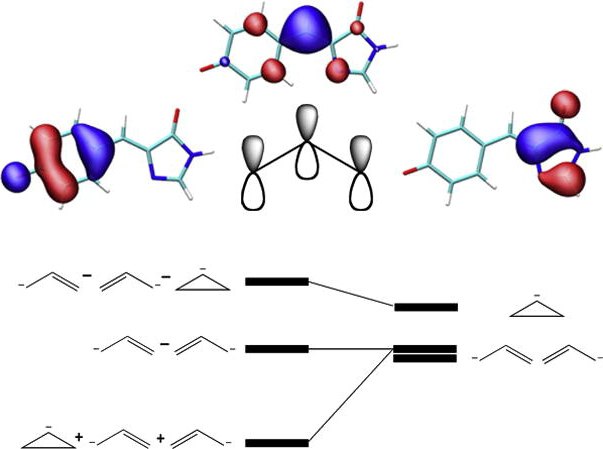
Elektronická povaha spojení je vysvětlena atomemvodík. Je známo, že obsahuje jeden nepárový elektron, který je na první energetické úrovni. Když se sbíhají dva atomy vodíku, jádro jednoho z nich začne přitahovat elektrony druhého a naopak. Interakce atomů probíhá mezi atomy, vzdálenost mezi nimi se snižuje, vzájemná přitažlivost je vyvažována odpuzováním jader. V právě vytvořené molekule se zvýší hustota elektronů.

Avšak ne všechny atomy vzájemně spolupracují. Takže elektronické pláště inertních plynů se nepřekrývají, tj. zůstávají stabilní. na toto pravidlo formulovány oktetů Lewis, který uvádí, že všechny atomy prvků v tvorbě chemických vazeb mají tendenci měnit elektronovou konfiguraci shell nejbližší inertního plynu, nebo tím, že připojí poskytující elektrony základě.

Na základě všech výše uvedených skutečností můžete udělatJe k závěru, že chemická vazba je interakce mezi atomy, ke které dochází při výměně elektronů nebo přechodu z jedné z elementárních částic materiálu do jiného.
</ p>
