Soda do pečiva: chemický vzorec. Chemický vzorec sody a jeho použití
Možná, každá domácí kuchyně má soda -nekonečná krabice s práškovitou látkou. Paní ho používají jako kulinární přísadu pro pečení. Rozsah jeho uplatnění je však tak široký, že látka může být volána s univerzální důvěrou jako univerzální asistent člověka. Ale co je soda? Jakým způsobem existuje a jak se používá v každodenním životě?

Názvy sody
Před tím, než přistoupíte k chemickým vlastnostem sodovky,stojí za zmínku, že jeho název - "soda", látka získaná z názvu továrny na omáčku soda, jejíž popel byl zdrojem sódy.
V chemii je sodík obecným názvem sodných solí kyseliny uhličité:
- Na2CO3 (uhličitan sodný) - chemický vzorec uhličitanu sodného;
- Na2CO310H2O - ekonomická soda;
- NaHCO3 - pečení sody. Jedná se o chemický vzorec sody;
- Na2CO3· H2O nebo Na2CO37H2O je chemický vzorec krystalické sody.
V každodenním i chemickém průmyslu existuje několik triviálních názvů látky:
- sóda na pečení;
- pitná soda;
- hydrogenuhličitan sodný;
- přísada E500;
- dekahydrát sodný.

Empirický vzorec
Chemický vzorec sody je NaHCO3. Jedná se o kyselou sůl kyseliny uhličité. Pokud přidáme atomové váhy všech jejích prvků, získáme atomovou hmotnost sody rovnající se 84 a. e.

Způsob, jakým je vytvořen, je velmi jednoduchý. Chemický vzorec sody je komplexní interakce hydroxidu sodného s kyselinou uhličitou:
NaOH + H2CO3 = NaHCO3 + H2O.
V oblasti chemie je hydrogenuhličitan sodný akomplex kationtu sodného a bikarbonátového aniontu. Když se tyto prvky zavádějí do těla, normalizují kyselé báze a neutralizují přebytek kyselin obsažených v kapalném médiu.
Kalcinovaná soda
Chemický vzorec uhličitanu sodného je Na2C03. Kalcinovaná soda je bílá, sypká látka, která může být ve formě granulí (A) nebo prášku (B).
Tento typ sodovky má řadu vlastností, které rozlišují sódu z jídla.
- pH média. Jak potraviny, tak uhličitan sodný jsou alkálie, ale první je slabý, pH je 8 a druhý silný, s pH = 11. Chemický vzorec technické sody je také indikátorem povahy média.
- Rozsah aplikace. Soda se používá v potravinářském průmyslu, kosmetice a medicíně. Kalcinovaný se používá jako účinný čisticí prostředek.
V domácnosti s pomocí uhličitanu sodného můžete:
- umyjte jej pomocí pracího prostředku;
- podlahové podlahy, ale pro laminát a parkety tento nástroj nebude fungovat, protože může poškodit povlak;
- odstranit blokování potrubí;
- k čištění výrobků z lahví.
Při použití uhličitanu sodného musíte být velmi opatrní, protože látka je velmi toxická, patří do třetí skupiny nebezpečných látek.

Fyzikální vlastnosti sody
Bikarbonát sodný je bílá prášková látka. Jedná se o komplex složek sodíku, vodíku, uhlíku a kyslíku.
Hustota prášku je 2,16 g / cm3.

S hodnotami teploty +50o-60oC se látka začne tát.
Bikarbonát sodný nebo sodná sůl jsou ve formě mléčného prášku. Je velmi rozpustný ve vodě. Nesvítí. Chemický vzorec pitné sody je stejný jako u potravin.
Sodný roztok

Soda do pečiva je látka, která se zcela rozpouští ve vodě, což vede k roztoku sody. Používá se pro hygienické účely jako prostředek pro oplachování ústní dutiny.
Chemický vzorec roztoku sodíku je následující:
NaHCO3 + H2O = H2CO3 + NaOH.
Vodný roztok sody je opatřen mírně zásaditým charakterem.
Hydrogenuhličitan sodný ve vodném roztoku se odděluje za vzniku následujících iontů:
Na2CO3 ↔ 2Na+ + C032-
Vlastnosti sody jako alkálie
Jak bylo opakovaně zmíněno, bikarbonátsodík je alkalická látka. Tato skutečnost ovlivňuje použití sody jako prostředku neutralizace zvýšené kyselosti těla, zejména žaludku. Prvky tvořící látku mají bezpečný účinek.
Soda zvyšuje účinnost ledvin, protožeVylučený moč má alkalické médium. Navíc uchovává potřebné množství glutaminu AK v těle, což zabraňuje vzniku kamenných formací v ledvinách.
Alkalické prostředí pomáhá lépe absorbovat některé vitaminy skupiny B: B1, B4, B5, B6 a B12.
Při použití sody pro dobrou asimilacikombinujte s horkým mlékem. To přispívá k tomu, že se tenké střevo soda reaguje s aminokyselinami mléka, což by mohlo mít za následek aminokyselina sodná sůl vykazující alkalický charakter. Tyto aminokyseliny jsou mnohem lepší než soda, pronikají do krevního oběhu, čímž zvyšují alkalické zásoby těla.
Louh sodný
Chemický vzorec hydroxidu sodného je NaOH. Strukturní vzorec: Na-O- H.
Molekulová hmotnost látky je tvořena atomovými závažími, tvořícími její složky Na, O a H. Je rovna 40.
Žíravina je velmi rozpustná ve vodě.
V průmyslu ve vztahu k tomuto typu sodovky se používají následující názvy:
- louh sodný;
- hydroxid sodný;
- hydrátu oxidu sodného.
Při práci s hydroxidem sodným je nutné používat ochranný oděv, protože při styku s pokožkou ponechává těžké popáleniny.
Soda v kombinaci s octem
Chemický vzorec octa a sody je kalení, při níž se vytváří voda, oxid uhličitý a kyselina octová.
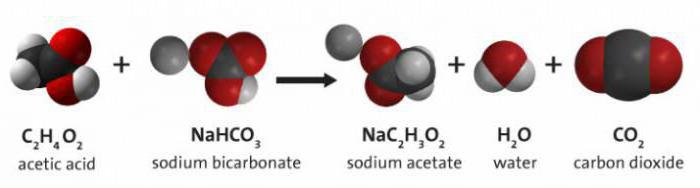
Tato chemická "zkušenost" je doprovázena charakterem, který naznačuje začátek "hoření" sody.
Taková reakce se provádí v kulinárním případě, kdyzamýšlejí těsto hnět pro pečení. Ocet pro tento přípravek se užívá v koncentraci 9%. Analogou kyseliny může být citronová šťáva, jablečný nebo vinný ocet.
Tak proč tuto reakci provádíte při přípravě testu? Věc je, že oxid uhličitý produkovaný rozkladem sodovky dává zkoušce nádheru.
Příprava látky
Jakmile byla soda vytažena z popelu rostlinysodíku. V současné době je základem pro získání této látky přírodní síran sodný. Reakce přípravku je následující, kde je chemický vzorec sody zobrazen vpravo:
Na2SO4 + 3C + 2O2 = 2Na2CO3 + CO2 + 2SO2;
CaCO3 + C + Na2SO4 = Na2CO3 + 4CO + CaS.
Použití sody na pečení
Soda je velmi populární v každodenním životě, a to nejen jako kulinářská složka. Podívejme se však podrobněji na případy použití sody.
- Pro začátek stojí za zmínku opět, že sodík -potravinářská složka v kulinárním podnikání. Jeho použití není náhodné: při zahřátí je látka schopná uvolňovat páru oxidu uhličitého, což zase dává zkušební vzdušnost. V tomto případě soda působí jako prášek do pečiva. Pokud však v obchodě zakoupíte sáček s otvírákem na pečení, pak na obalu v linii složení zjistíte přítomnost sody, která je označena jako doplněk stravy E500.
- Použijte sódu na pečení a pro výrobu sýrových nápojů.
- Velmi často se soda používá v tzv"Lidový" lék. V této oblasti je sóda všelékem téměř všech onemocnění, například její účinnost je prokázána pálením záhy, kašlem, bolestí v krku, žaludkem, při zvýšené teplotě.
- Dobrá pivovarská soda a jako čisticí prostředekprostředky. Můžete jej použít k čištění klempířských, hliníkových hrnců, nádobí, koberců, stříbra a pro praní prádla. Látka má dobrou dezinfekční a protiplesňovou látku.
- Mnoho žen užívá sódu a v kosmeticea pro hygienické účely. Lze ji použít jako křovinu kůže. Produkt bude dokonale odstraňovat drsnou pokožku nohou, pokud se používá pro noční lázně. S její pomocí se můžete zbavit zápachu potu v podpaží i botách.
Pomůže sójové a bílé zuby. Je to levný, ale efektivní způsob. Sodný prášek se mísí s čištěním zubní pasty nebo vodou a jemnými zuby.
Louh sodný: aplikace
Použití tohoto typu sody by mělo být spojeno s určitými bezpečnostními opatřeními, jako žíravina - silnou zásadou, která může „užírat“ mnoho typů povrchů.
Proč může být louhový prostředek užitečný v domácím prostředí?
- Kaučuk se dokonale vyrovná s různýmiznečištění na nádobí. Ale měli byste se zdržovat používání tohoto nářadí pro výrobky vyrobené z hliníku a teflonu. Ale pro zbytek kelímků, pánve nebo pečení - prosím. Nagar, spodina, staré vrstvy tuku - se všemi těmito látkami se snadno vyrovnává žíravina.
- Louh sodný může vyřešit problém ucpaných trubek. Je nutné jednoduše naplnit zrnitou látku do potrubí a chvíli ji nechat, poté opláchnout tekoucí vodou.
Žíravá soda, také žíravina, je široce použitelná na průmyslové úrovni v různých oblastech výroby.
- Ve výstavbě. Zde se látka používá k výrobě některých typů stavebních materiálů a slouží také jako dodatečná součást, která posiluje základní strukturu.
- V potravinářském průmyslu. Louh sodný je také použitelný při výrobě potravin. Samozřejmě, že v tomto případě je používán ve slabé koncentraci. S její účastí, kakaovým práškem a čokoládou, zmrzlinou, karamelem, chlebem se pečeme, používá se jako přísada E524.
- Textilní průmysl. V této oblasti je louh sodný užitečný při bělení tkanin a při regeneraci pryžových výrobků.
- Chemická výroba: louh sodný se používá jako neutralizátor kyseliny, prostředek pro čištění oleje a výrobků na něm založených. Výroba technických olejů se také nedá provést bez přidání louhu sodného. Navíc louh sodný je dobrým katalyzátorem pro některé chemické reakce.
- Aplikovaná hydroxid sodný a pro výrobu mýdla při výrobě různých typů mýdel, šamponů a gelů.
Kalcinovaná soda: použijte
Kalcinovaná soda se nazývá také prádlo. Zvláštní prostředky tohoto nástroje používané v Sovětském svazu, můžete tedy říci: lněná soda je testována časem.
Nástroj se používá v následujících situacích:
- Během umývání věcí.
- Při čištění povrchů dlaždic, keramiky, fajánů.
- Při odstraňování blokády v potrubí.
- Pro odstranění stupnice v bubnech praček i na nádobí.
- Pro zničení škodlivého hmyzu v kuchyňských zahradách.
Z výše uvedeného vyplývá závěr: soda je univerzální nástroj používaný ve většině oblastí domácího i průmyslového života.
Pozitivní kvalita látky spočívá v tom, že ji lze zakoupit za penny.
</ p>


